单细胞转录组测序分析揭示EGFR突变肺腺瘤中抑制性免疫肿瘤微环境

达普生物品牌馆
2022-09-26点击量:
肿瘤微环境是肿瘤细胞存在的周围微环境,包括周围的血管、免疫细胞、成纤维细胞、骨髓源性炎性细胞、各种信号分子和细胞外基质(ECM)。肿瘤微环境对肿瘤的免疫抑制,耐药,肿瘤侵袭,转移生长等发挥着至关重要的作用。
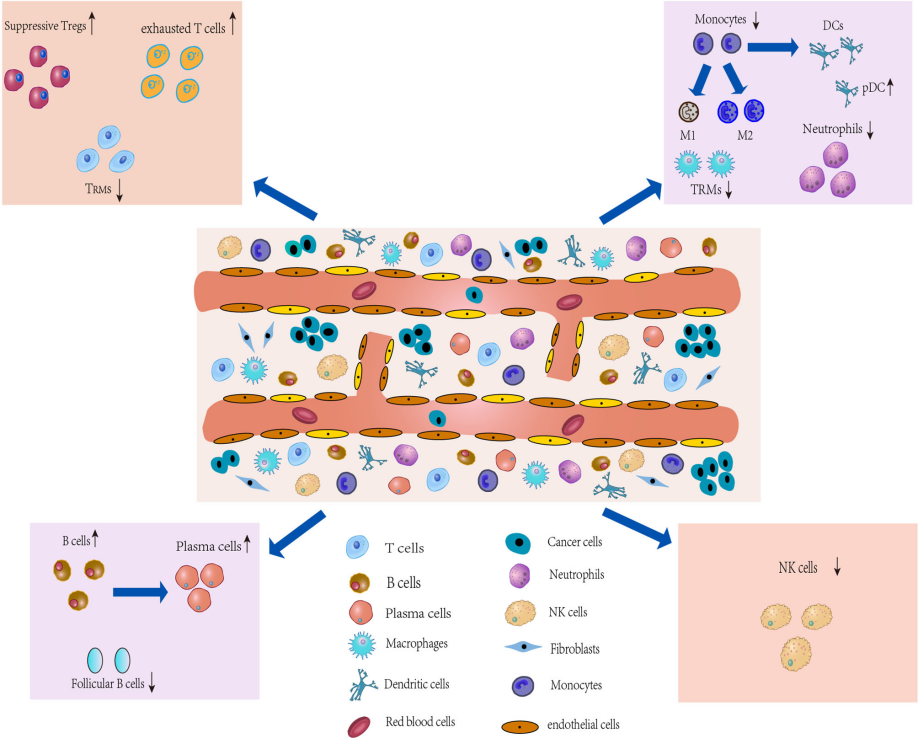
图 1. 肿瘤微环境特征
单细胞转录组测序是深入探索 EGFR 突变肺腺瘤中抑制性免疫肿瘤微环境的利器。

1、上皮细胞驱动肿瘤微环境的多样性。 2、B 细胞在 EGFR 阴性 LUAD 的 TME 中促进 TLS 的形成。 3、细胞间相互作用因 EGFR 状态的不同而不同。
“肿瘤”是一个复杂的生态系统,以往研究表明,EGFR 突变型肺腺癌(EGFR-LUAD)的肿瘤突变负荷(TMB)较低,免疫治疗疗效不佳,且 EGFR-LUAD 的免疫微环境(TME)尚不清楚,这都为该疾病的治疗增加了难度。到目前为止,肿瘤微环境(TME)在 EGFR 突变患者免疫治疗中的研究还不全面。
据此,杨蕾博士和其团队发表了一篇题目为 “Single-cell transcriptome analysis revealed a sup/p/ssive tumor immune microenvironment in EGFR mutant lung adenocarcinoma” 的文章。该文章运用单细胞转录组测序(scRNA-seq)的分析方法,从细胞组成和功能的角度,揭示了 EGFR 突变型肺腺癌(LUAD)的特异性肿瘤微环境(TME),其研究成果发表于《Journal for ImmunoTherapy of Cancer》杂志上(IF=13.751),为 EGFR 突变 LUAD 患者的治疗提供了理论基础和新思路。


1、样本信息:
8 名患者的 9 份 LUAD 肿瘤组织,5 份 EGFR 突变型,4 份 EGFR 野生型样本。
2、实验流程:
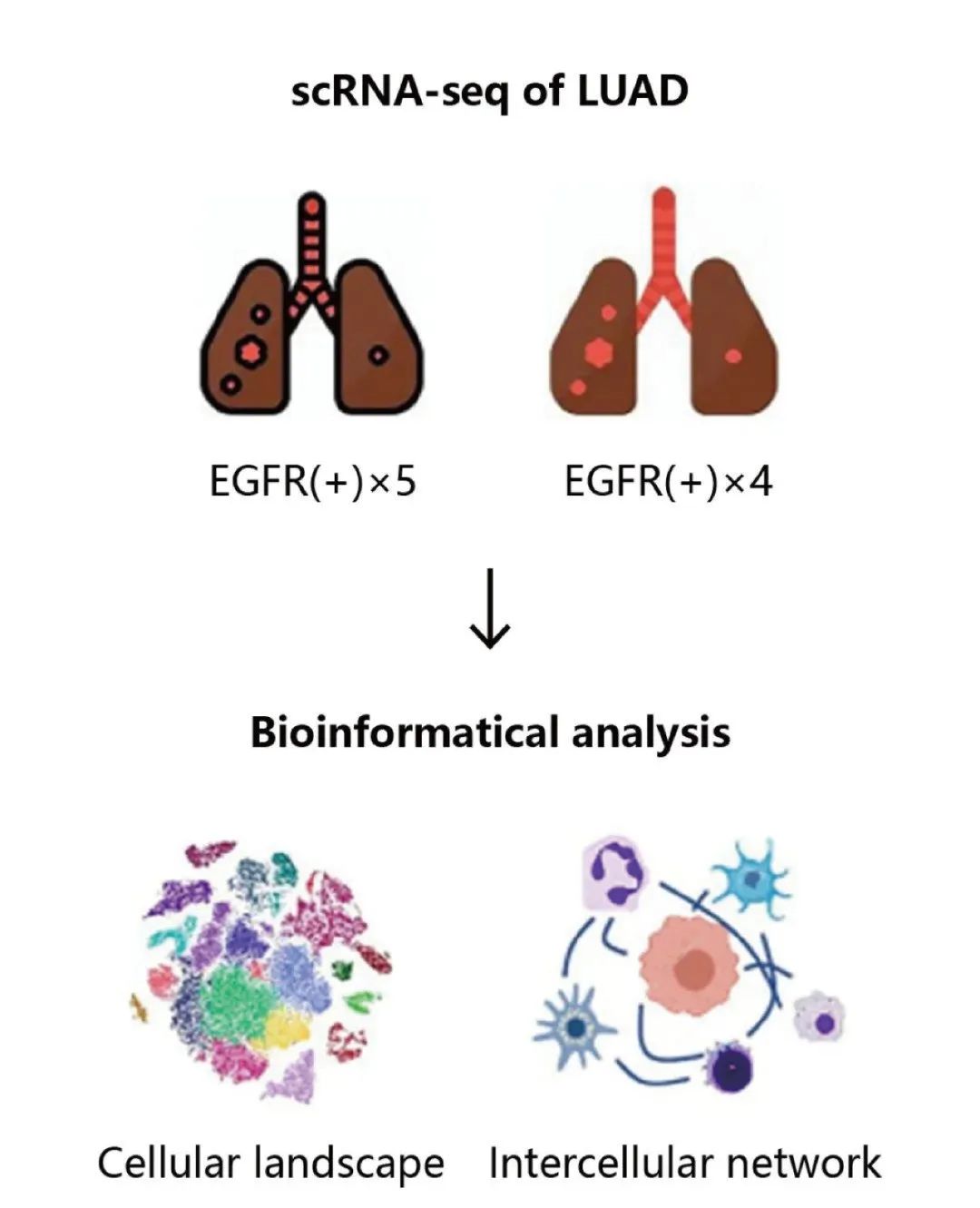
图 2. 样本信息、实验设计流程示意图

对获得的 9067 个上皮细胞分析,基于拷贝数变异信息将其分为肿瘤细胞和正常细胞,并最终得到 13 个细胞亚群( 10 个肿瘤细胞亚群,3 个正常细胞亚群)。根据差异丰度测序分析,EGFR 阳性组细胞亚群 1 和 5 特异富集 ,EGFR 阴性组细胞亚群 0、6、8 和 11特异富集 。
推测:EGFR 阴性肿瘤细胞可能比突变的肿瘤细胞更能促进 CD8+ T 细胞的增殖和功能。
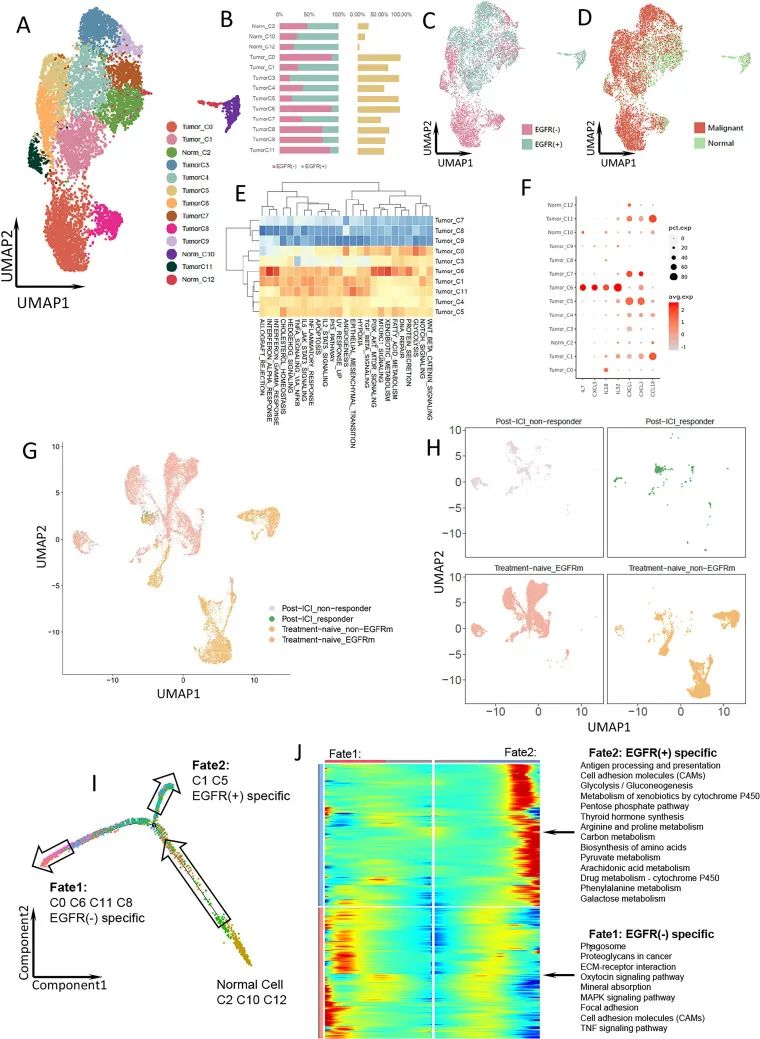
图 3. 在 LUAD 中具有不同 EGFR 突变状态的上皮细胞
提取 T 细胞进行细分,发 现CD8+ 组织细胞在 EGFR 阴性组中较高,CD103 是 TRM 细胞表面表达的标志物,且 CD103+CD8+ TRM 细胞与多种癌症免疫治疗后生存率的提高有关,后续的 mIHC 结果也显示 EGFR 阴性组 CD103+CD8+ T 细胞比例更高。
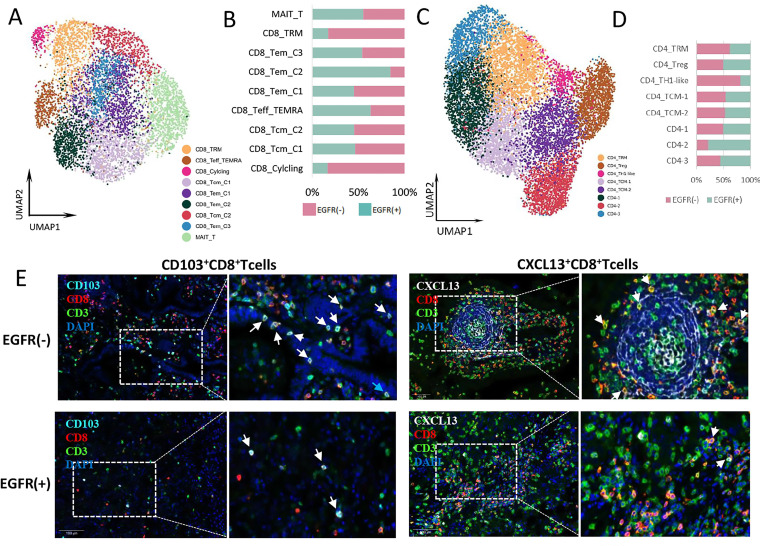
图 4. LUAD 中的 T 细胞和 NK 细胞簇
对 T 细胞分泌细胞因子研究,发现 CD8+ TRM 中 CXCL13 的表达更高。CXCL13 可介导肿瘤对 B 细胞的招募,并对三级淋巴结构(TLS)的形成至关重要,TLS 是癌症对免疫治疗反应的积极预测因素。mIHC 结果也显示 EGFR 阳性组的 T 细胞表达更多的免疫抑制细胞因子。总体,单细胞测序结果显示:EGFR 阳性 LUAD 的 T 细胞中 CD8+ TRM 细胞缺失,CXCL13 表达降低,免疫抑制因子表达却升高,这提示 EGFR 突变对 TME 有负向修饰作用。
B 细胞是 TLS 最重要和最基本的组成部分。细胞与细胞相互作用分析显示,表达 CCR7 的 B 细胞可与表达 CCL21 的肿瘤巨噬细胞互作,而 CCR7 在 EGFR 阴性组的B细胞中表达较高,综合之前一些报导的数据,总体表明来自 EGFR 阴性组的B细胞可能已被肿瘤巨噬细胞招募,并具有在肿瘤微环境中构建 TLS 的潜力。
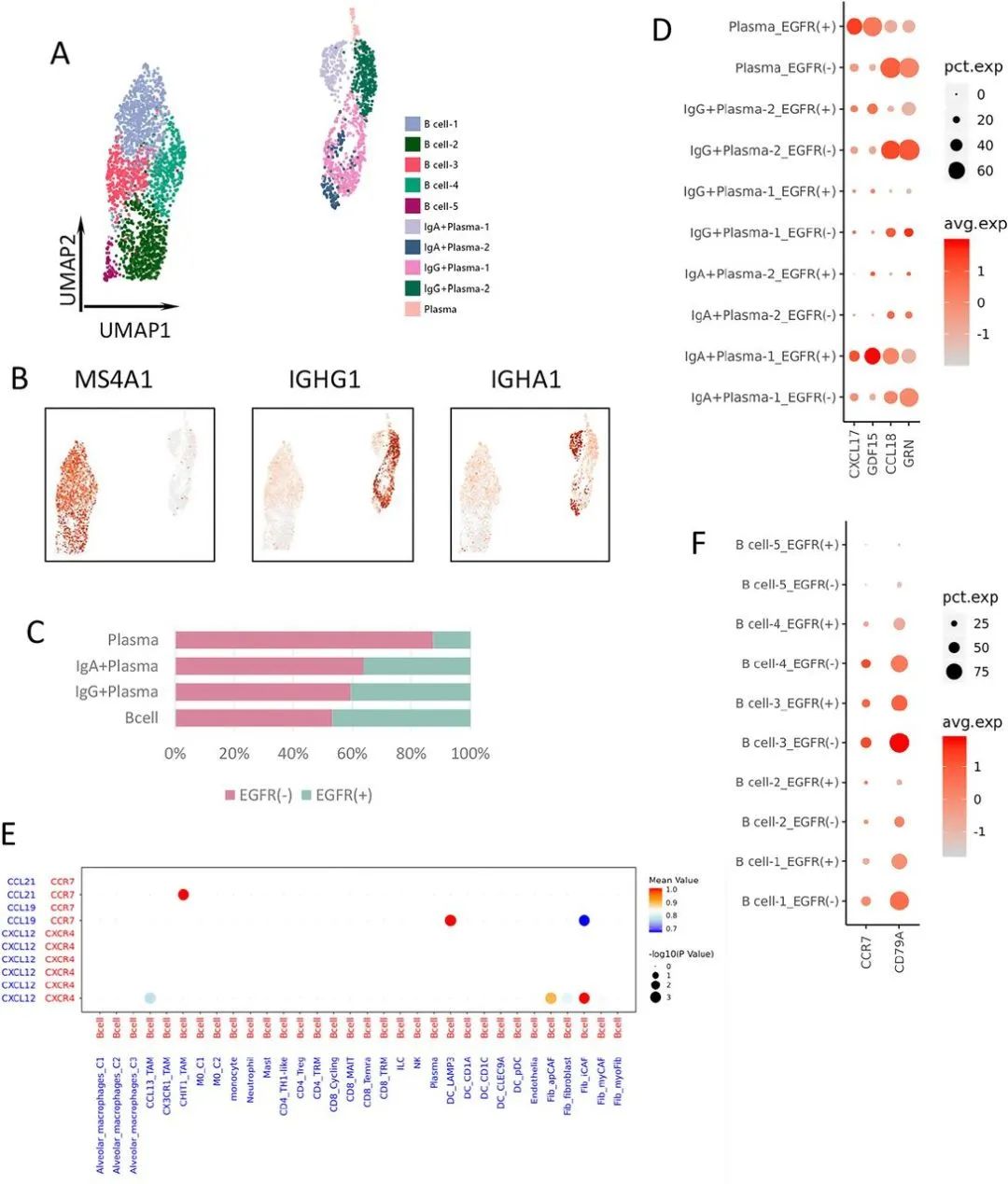
图 5. B 细胞聚类和差异基因表达
对 LUAD-TM 中的细胞相互作用分析,发现两个特异性细胞亚群之间的配体-受体结合对在 EGFR 阴性组和阳性组中存在差异:有些配对在两组中均存在,而有些仅在 EGFR 阴性组或阳性组中出现。结果可能为 EGFR 突变 LUAD 的免疫治疗提供新的思路。
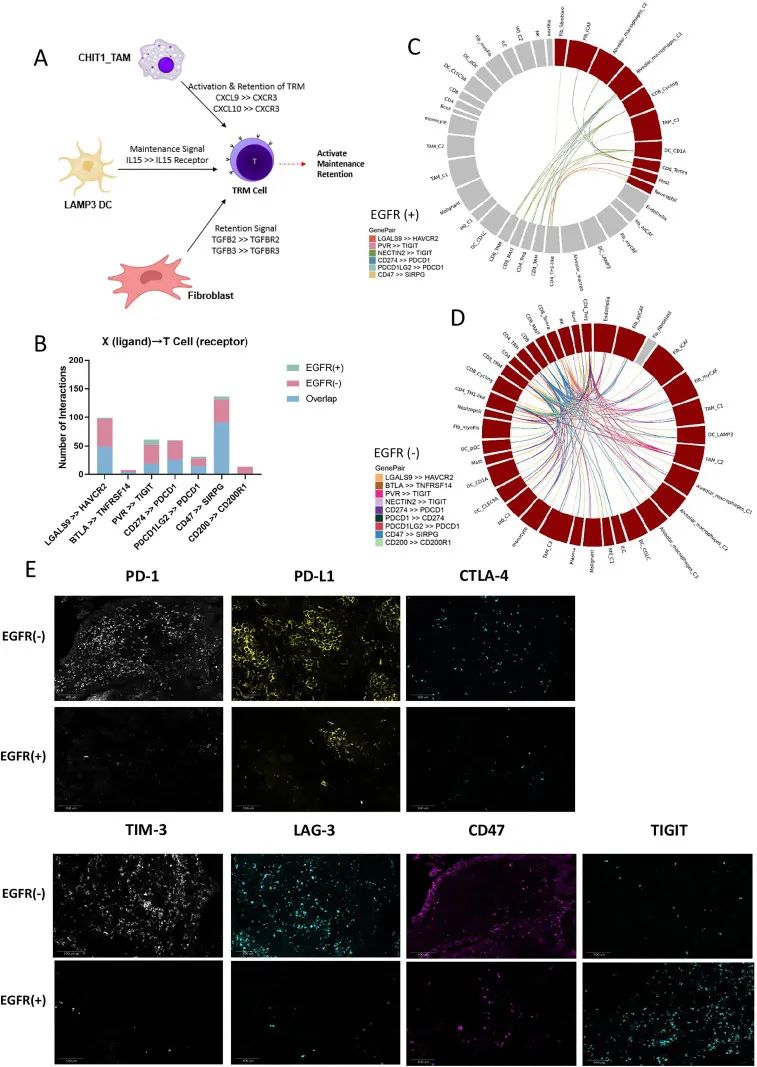
图 6. EGFR 突变状态决定宏观表达差异

本研究从单细胞层面上阐释了 EGFR 突变型和野生型 LUADs 肿瘤微环境的细胞组成和相互作用的异质性,EGFR 突变型 LUAD 与 EGFR 野生型 LUAD 具有截然不同的特异性 TME。肿瘤细胞的 EGFR 基因可能通过直接或间接改变 TME 周围不同类型细胞之间的通讯,从而在 TME 构建中起决定性作用。
作者将公开发表的免疫治疗后样本的 scRNA-seq 数据与自己未经治疗样本的数据进行了比较,并且进行了 mIHC 以加强研究结果的可信度,以此揭示未来 EGFR 突变型 LUAD 免疫治疗的一些潜在方向。未来可考虑对 EGFR 突变型 LUAD 进行联合免疫治疗,以改善抑制性肿瘤免疫微环境。

作为行业国产化的积极参与者,达普生物秉承为广大科研及临床工作者和企业客户提供世界领先技术平台的理念,达普生物全流程自主研发,创新性开发了基于微流控的单细胞测序解决方案产品 —— Galaxy 星海单细胞建库系统 ,该技术克服了传统技术低通量、高成本、高技术门槛的弊端,以国产化的仪器与试剂,为单细胞测序技术在肿瘤学及精准医学应用中扫除障碍。
Galaxy 星海单细胞建库系统可在几分钟内分离数百至数万个单细胞用于文库构建,实现单个细胞水平的高灵敏基因检测。1-4 个样本的灵活上样设计,解决长久以来单细胞测序成本浪费的问题。系统兼容转录组、TCR/BCR、ATAC、CUT&Tag 等文库构建,同时匹配市面上如 T7、GenoLab M、NovaSeq 等主流测序平台,全方位解决肿瘤学及精准医学中单细胞测序从文库制备到测序过程的烦恼!
性能优:可一次性完成数百至数万个细胞的分离,基因检测灵敏度高。 上样活:1-4 通道,可灵活选择样本数及细胞数量,方便快捷。 兼容好:文库兼容目前不同的主流测序平台。 分析全:自主开发的 StarScope 生信分析软件,可完整从原始数据到分析报告的生信分析。 流程活:可接驳下游流程 ,如单液滴分选。 多应用:3'mRNA kit,TCR/BCR kit,ATAC,CUT-TAG 等kit。
参考文献:Single-cell transcriptome analysis revealed a sup/p/ssive tumor immune microenvironment in EGFR mutant lung adenocarcinoma, J Immunother Cancer 2022.



